ДРУГИ СЕМИНАРСКИ РАБОТИ
- МЕДИЦИНА: |
||||||||||||||||||||
|
||||||||||||||||||||
Генетски аспекти на мултиплекс склероза
Мултиплекс склероза и други демиелизирачки заболувањаЛуѓето се измачуваат со два главни типа на демиелинизирачки заболувања. Првата група ги опфаќа едно-генските заболувања, во кои клиничкото манифестирање е независно од амбиентските фактори. Примери се леукодистрофиите, во кои демиелинацијата влијае на централниот нервен систем (CNS) и периферните нерви. Овие услови обично се случуваат во раното детство или во детството и дава конзистентна клиничка слика. Наследството е автосомно рецисивно. Постојат две врзани демиелизирачки леукодистрофии: Pelizaeus-Merzbacher болест и адренолеукодистрофија. Другите едно-генски заболувања опфаќаат демиелински периферни невропатии.
Втората група се состои од оние демиелински болести што изгледа се предизвикани од меѓудејството на еден или повеќе амбиентни предизвикувачи (пр. инфекција или вакцинација) и состојбата на имунитетот на пациентот.
Разноврсност на демиелинизирачки заболувања може да биде продуцирана кај животните во завизност од два збира на етиолошки фактори: антигенски стимуланс презентиран под специфични услови и посебен вид на лабараториско животно (Raine and Traugott, 1984; Waksman and Reynolds, 1984). Реакциите на животните може да резултираат во една акутна или хронична болест. Антигенскиот стимуланс обично произлегува од миелинот. Неговиот медиум, тајмингот и положбата на инектирање се важни; понекогаш е потребна претходна вирусна имунизација. Овие предизвикувачи доведуваат до серија на имунолошки настани кои се состојат од автоимуни демиелинизирачки процес посредуван низ Т лимфоцити и хистокомпатабилни антигени и здружени со производството на антитела до миелински протеини. Во многу врсти на глувци и заморчиња ова е акутна самолимитирачка болест, само неколку врсти на лабараториски животни (пр. Врста 13 заморчиња и SLJ/J глувци) реагираат на горниот тип на стимулант со хронично демиелинско заболување.
Освен тоа, особено е интересно што SLJ глувците можат да развијат хронична повратна демиелинска болест после имунизација само со замотани вируси и што глувците покажуваат докази на осетливост на миелински антигени (Waksman and Reynolds, 1984).
Демиелинските заболувања на лабараториските животни се обично форми на енцефалитис но во најново време се индуцирани неуропати. Тие имаат воочливи соодветности како кај човечките болести, како акутен алергичен енцефалитис следејќи инфекција иливакцинација, акутен Guillain-Barre A-синдром и хронични болести од кои мултипна склерозата (МС) е најопшт пример.
МУЛТИПЛЕКС CKJIEPO3AМС е болест при која се појавува мултипли плакови на демиелинација во CNS заедно со астроцитоза и зголемена пропустливост на малите садови (McDonald, 1987). Оваа патолошка нееднаквост се одразува на клиничките својства што варираат на време и место.
Почетокот на МС е главно на возраст од 20-55 години. На млади години состојбата е поопшта кај жените (Kurtzke, 1983). МС може да оди по еден од двата тека: еден повратен или повратен и прогресивен; и една хронична форма која е немилосрдно прогресивна. Повратната форма има опран почеток, достигнувајќи врв од 20-40 годишна возраст, додека хроничната форма достигнува врв со почетокот на 30-55 годишна возраст. Во една студија во Норвешка, (Larsen at al. 1985) забележал дека има пораст на повратната форма во последните 30 години, но никаква пратечка промена во случајот на прогресивната форма. Овој пронајдок ги води истражувачите и ги наведува да сугерираат дека етиологијата на двата типа може да биде различна; постојат имунолошки разлики во подршката на оваа сугестија. Во Јапонија каде МС е ретка, повратната форма е поопшта меѓу жените (Shibasaki and Kuroiwa, 1976), опсервација што е веројатно главна карактеристика на области со малку случаи (Achenson, 1985).
Дијагнозата на МС е направена врз основа на клинички опсервации на симптоми и знаци распространети во време и место.
Со евиденција на демиелинација врз визуелно предизвикани реакции или MRI (каде карактеристичните својства се повеќе од една високоинтензитетна област во белата супстанца на мозокот) и од присуство на олигоклонални траки во цереброспиналниот флуид (CSF).
Дијагностички критериуми се дадени од Poster et al. (1983) and Paty et al. (1988). Патолошки, плаковите не демиелинација се поврзани со предизвикувачки инфилтрати; има вишок и различни антитела на ендотелни келии во CNS, вклучувајќи антитела до миелински базен протеин и милеински олигодендроцит гликопротеин.
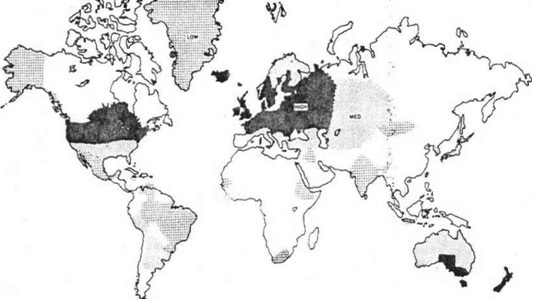
МС има различна распространетост во различни делови на светот. Главно, распространетоста се зголемува со геограФската широчина и на северната и на јужната хемисвера. Скандинавија и Оркни и Шетланд островите покажуваат големо преовладување. Глобално, Северните Европејци имаат ризик од МС 100 20-пати поголем од оној на другите популации. Спротивно на тоа, Јапонците Унгарските цигани и староседелците на Нов Зеланд имаат особено низок домен на болест.
2. Медицински аспекти на Мултиплекс склероза2.1 Етиологија на МС
Етиологијата и патогенезата на оваа болести до ден денес останале непознати. Кај лицата со МС може да биде нагласена анамнеза за алергија. Тоа може да биде ОСЕТЛИВОСТ на вируси, бактерии и вакцини. Титар антителата на морбили секогаш ги има нешто повеќе кај лицата со МС, но епидемиолошките податоци во врска со морбилите и нивната геограФска распространетост не се сложуваат со податоците за МС. инфективната етиологија на МС е атрактивна хипотеза, посебно онаа за инфекции со спори вируси. Денес се обраќа внимание на тоа дека всушност примарната инфекција се случува уште во раното детство, после која настанал интервал на мирување коЈ траел со години. Тоа доведува до заклучок дека болеста може да биде латентна со години или пак цел живот, или до тогаш се додека некое влијание од надворешната средина не ги предизвикаат мртвите симптоми.
Болните од МС имаат зголемено ниво на гама-глобулин во ликворот. Зголемениот IgE е значаен ако е поголем од 14% од вкупните протеини во ликворот. Ова се забележува во 66% кај случаите со МС. Во серумот IgE е нормален или значително зголемен. Најдено е дека болните од МС имаат нормална реакција на неспецифичниот митоген Phutohaemaggeutinin M и на специфични митогени антигени, стрептолизин и стрептокинеза-стрептодорназа. Според некои сознанија МС може да е последица на автоимунизација. Во прилог на тоа зборува и зголеменото количество на гама-глобулин во ликворот. Се претпоставува дека кај МС постојат антитела на нервното ткиво. Раната инфекција создала преосетливост на инфективниот агенс или на автогените антигени. Кога со подоцнежна инфекција ке се ослободи оваа компонента, може да се создаде автоимуна реакција на местото на нејзиното ослободување и создава демиелинизација. Траумата понекогаш може да биде прецепитирачки фактор.
Тоа посебно се поклопува со местото на траумата и појавата на првите знаци на болеста (пр. повреда на шаката и сензитивни промени неколку часови или денови подоцна). Кај некој луѓе постојат јасни податоци за психички потреси пред да се јави болеста. Понекогаш заморот и напрегнувањето може да бидат повод за започнување на болеста. Забележани се случаи кои започнуваат после акутна инфекција, за време на бременоста и лактацијата, после операции и трауми. Општо е мислењето дека овие фактори ја фаворизираат појавата на болеста.
Како етиолошки фактори се наведува и тромбозата во малите вени на CNS, интоксикации со олово, недоволно внесување на бакар, храна богата со масти итн.
2.2 Клиничка слика на МСКласичниот Шаркотов тријас ни укажува на клиничката слика на МС: нистагмус, интЕнционен тремор и скандиран говор. Во класичниот опис на клиничката слика спаѓа и спастичко-атаксичното одење.
Болеста најчесто почнува со појава на едно или повеќе жаришни знакови кои траат извесно време па се губат потполно или оставаат зад себе некои траги.
Меѓу првите знаци може да бидат: скотомите или нејасниот вид кои за неколку дена се развиваат во слепило.
Кај МС најчесто се работи за ретробулбарен неуритис кој не дава промена на очното дно. По извесно време видот потполно се подобрува и ремисијата може да трае со години.
Болеста може да почне со моторни знаци: спастичка парапареза, хелиплегија или моноплегија, а може и да се јави парализа на периферниот фацијален нерв.
Оштетување на сензибилитетот е еден од првите симптоми на болеста. Неуралгија на u.tugeminus може да биде симптом на МС.
Нистагмусот може да настане на почетокот на болеста, понекогаш следен со вртоглавици и може да трае со недели.
интенциониот тремор исто така е често присутен знак во понатамошниот тек на болеста. Во случаевите на МС се забележува и скандиран "staccato" говор, со издвојување на некои слогови или дизартричен.
Пореметувањето на свинктериите можат да бидат минливи или во некои случаи се трајни. Често болните се или еуфорични или премногу депресивни. За оваа болест е карактеристично променливо однесување.
2.3 Диференцијална дијагнозаВо типичните случаи кога може да се констатираат жариштата на болеста, во случаи на ремисија и егзацербации, дијагнозата лесно се поставува.
Тешкотија во дијагностицирањето претставуваат случаевите кои асоцираат на миелитис или пак ако развојот на параплегијата е постепен тогаш асоцира на компресија на рбетниот столб.
Понекогаш, цервикалната спондилоза може да има слични симптоми со МС. Во такви случаеви потребни се дополнителни дијагностички методи.
Конечно, многу заболувања покажуваат слични симптоми како и МС, затоа и асоцираат на истата. Поради тоа стручњаците превземаат дополнителни методи со цел да се уверат дали се работи за МС.
2.4 Лекување на МСЛакувањето на МС се менувало спрема сваќањата за етиологијата на оваа болест. Пробувано е антисифилисно лекување, пиретотерапија, лекување со туберкулостатици, витамини Б1 и Б12 и со многу други лекови.
Подобри резултати се добиваат кога се лекува со АСТН (60-80 единици депоинекција секојдневно две недели, потоа една недела 40-единици и уште една недела со 20-единици дневно). Пронисон се дава во доза од 80мг дневно 3-4 недели, по него наизменично секој втор ден се дава АСТН. Долгото лечење со кортикостероиди може да доведе до атрофија кората на надбубрежната жлезда.
Лекувањето со антиметаболитите дава добри резултати (Purinethioe, cytosin-arabinosid-c, Methotrexat). Може да се даде и валиум за лечење на спастичката хипертонија. За вртоглавици се препорачуваат соодветни седативи.
3. Фамилијарни студии
Прво, фамилијарните проучувања покажаа дека преовладувањето кај сопрузите е иста како кај главната популација (Shapira et al., 1963), така било какво дејство на општата средина во зголемување на ризиците на враќање кај роднините на се проширува во животот на возрасните. Проучувањата за другите роднини се сумирани во Табела1. Набљудувањата се однесуваат на преовладување на МС може да се споредат со преовладувањето на населението; всушност сите овие студии беа правени во области со високи случаи. За родителите и родените браќа или сестри, резултатите веројатно ќе бидат споредливи, додека повеќето истражувачи имаат направено подесување за младите возрасти на децата. Преовладивоста кај браќата или сестрите од околу 1¬2% и е значително поголема отколку онаа кај населението. Преовладувањето кај родителите е пониско, но ова може веројојатно да се објасни со редуцираната веројатност на еден пациент со МС да стане родител. Преовладливоста кај децата е слична со онаа кај родените браќа или сестри, ако се земе во обзир староста, а преовладливоста кај роднините од втор и трет степен е многу пониска, иако сеуште значителна над преовладливоста на населението.
Враќањето на МС кај родените браќа или сестри се зголемува на 5% ако две роднини од прв степен се заразени (Millar and Alison, 1954) е уште поголемо ако неколку роднини се заразени (Hartung et al., 1988). Генетичките податоци наведуваат полигено наследство од три причини.
Прво, ризикот за членовите на фамилијата е помалку зголемен во однос на ризикот на населението во областите со многу висока преовладливост, споредено со областите со ниска преовладливост. На пример, во Оркни, каде што преовладливоста на населението е 1 во 342, ризикот на роднините од прв степен е 4 пати поголем од ризикот на населението (Roberts et al., 1979), за споредба, ризикот кај роднините од прв степен во Ванкувер е 20 пати поголем од преовладливоста на населението од 1 во 10000.
Второ, значително зголемениот ризик за роднините од прв степен е редуциран за роднините од втор степен и е помал повторно за роднините од трет степен.
Трето, ризикот за родените браќа или сестри и младите се зголемува ако повеќе до еден близок роднина е заразен.
На претпоставка дека генетичката можност за МС е полигена, тоа е за да се пресмета наследувањето со што се мери одастапувањето во можноста поради фамилијарните фактори. Фактот дека наследувањето пресметано за роднините од втор и трет степен е слична на онаа пресметана од роднините од прв степен (Roberts and Batest, 1982) установува дополнителен доказ дека полигениот модел е точен.
Наследувањето е конзистентно повисоко кај родените браќа или сестри одколку кај родителите: 56-57% споредено со 40-48% (Berry, 1969, Roberts et al., 1979). Ова би можело да значи дека поделената средина на родените браќа или сестри е важна етиолошки или дека овие разлики го рефлектираат фактот дека пациентите со МС е помалку вЕРојантно да станат родители одклоку здравите поединци.
Единственото набљудување кое не се согласува со полигеното наследство се однесува на споредба на ризици на роднини од машки и женски пациенти. Треба да се очекува дека пациентите од помалку заразениот род (во овој случај машкиот) би им давале поголеми генетски ризици на нивните роднини отколку што би давале пациентите од поопширно заразениот род.
4. Студии за близнаци
Студиите за близнаци се многу фасцинантни за неурологистите, надвор од пропорцијата на нивната вредност. Постојат многу студии на МС за близнаците, и овие прво покажале дека близнаците по себе, биле монозиготните (МЗ) или дизиготните (ДЗ) немаат зголемена можност за МС, бидејќи преовладливоста кај близнаците е исто како за главното население. Студиите за близнаците се сумирани во Табела 2, кои претставуваат различни податоци. Некои (Maskay and Myrianthopoulos, 1966, Williams et al., 1980) ги најдоа нивните близнаци по оглас, други користеа регистер на близнаци (Heltberg and Holm, 1982) или регистер на воени ветерани (Bobowick et al., 1978), други сеуште користат една или повеќе болнички клиники. Двете најголеми болнички студии се оние изведени од Ebers et al. (1986; лична комуникација, 1987) со податоци од десет МС клиники во Канада и од Mumford et al. (1994; лична комуникација, 1994) со податоци од Обединетото Кралство.
Комбинирањето на сите студии за близнаци, покрај нивните разлики, дава сеопфатНА согласност за МЗ близнаците од 25% и околу 5% за ДЗ близнаците. Користејќи ги овие истражувања, претпоставувајќи нормална дистрибуција на една основна генетичка предиспозиција, може да се пресмета наследливоста (Табела 3). Проценките на наследливост кои произлегуваат од корелација за можност се 72% за МЗ близнаците, а 86% за ДЗ близнаците. Овие проценки се значително поголеми од проценките на наследливост од 56-57% произлезени од преовладливостите кај родените браќа или сестри и наведуваат дека сличната средина делена од близнаците на идентична возраст мора да придонесува кон нивната целокупна фенотипна варијација. Може да се направи попуштање за ова со корекција со која се претпоставува дека компонентата на средината е иста за МЗ како и за ДЗ близнаците. Кога ова ќе се направи, проценката на наследивоста станува 58% што е поблиску до онаа добиена од родените браќа или сестри. Една споредба на преовладливоста на МС кај ДЗ близнаците и кај родените браќа или сестри (James, 1985) покажува дека преовладливоста и наследливоста кај ДЗ близнаците кои се генетички слични со родените браќа или сестри, се значително поголеми од оние кај родените браќа или сестри, со исклучок на студијата од Ebers et al., (1986).
Ова набљудување обезбедува понатаму доказ за важноста на поделената средина во зависност од староста во детството.
Не е можно да се направи точна проценка за доприносот направен од поделената средина, бидејќи се присутни други збунувачки фактори, како родот и постоењето на доминантно наследениот HLA-поврзан предиспонирачки ген кој има поголемо дејство кај женските отколку кај машките. Меѓутоа, евиденцијата од МЗ близнаците сугерира дека поделените настани во детството (пр. извесни инфекции, во извесен ред на извесна возраст) допринесуваат кон развојот на МС кај МЗ коблизнаците.
5. HLA асоцијации
Здружување на извесни HLA алели со МС беше прво забележано во текот на 1970-тите (сумирано од Jersild et al., 1975). Наскоро станало јасно дека најјакото здружување било со HLA-DR2 (Batchelor et al., 1978), давајќи релативен ризик од 10 и дека првите здружувања што се најдени со HLA-A3 и B7 се должни на спојниот дисеквилибриум со DR2. Не е изненадувачко да се најдат различни асоцијации опишани кај други раси, бидејќи постојат расни разлики во дистрибуцијата на HLA алелите.
Најјакиот доказ за постоењето на HLA-поврзан предиспонирачки ген за МС доаѓа од студиите на HLA хаплотипови во заразени парови на родени браќа или сестри и парови на роднини (Ho et al., 1982 ; Stewart and Kirk, 1983). Ако гените во HLA регион не играат никаква улога во развојот на МС, дистрибуцијата на хаплотиповите кај заразените родени браќа или сестри би била ретка, со 25% од заразените браќа или сестри HLA идентични и 50% кои делат еден хаплотип. Ако, од друга страна еден ген во HLA регионот бил битен за развој на МС и доминантен, 50% од заразените браќа или сестри би биле HLA идентични а 50% би делеле еден хаплотип. Забележаните проценити кај 222 парови на родени браќа или сестри се 40% и 47% соодветно значително различни од случајните.
Stwart et al., (1981) исто така ги анализирал HLA хаплотипите кај парови на заразени роднини изнесени во литературата. Една третина од овие парови треба да делат еден хаплотип, а три четвртини не треба да делат ни еден.
Всушност, 10 од 17 парови делат еден HLA хаплотип, што е значително различно од очекуваното, а обезбедува понатамошна евиденција за еден или повеќе HLA-поврзани предиспонирачки гени.
Интересно е што HLA-поврзаните гени се етиолошки поважни кај жените одколку кај мажите, ситуација аналогна на онаа најдена кај мѕастхенија гравис. Ова било прво применето од Weitkamp (1983) кој забележал дека заразените сестра-сестра парови ги делат двата хаплотипи во 78% од примерите, додека заразените брат-брат парови делат хаплотипи многу помалку.
Посматрањето дека околу 13% од заразените парови на родени браќа или сестри не делат ни еден HLA хаплотип е еден дел од евиденцијата дека HLA-поврзаниот ген не е бите на развојот на МС; друго е што во некој области нема здружување со HLA хаплотип. Еден таков пример е во Оркни и Шетланд островите, каде МС е општа, но населивоста на областа е релативно ниска (Roberts et al., 1979, Poskanzer et al., 1980). Објаснувањето за ова посматрање е што факторите на средината во Оркни и Шетланд се поважни од генетичките фактори.
Модерните молекуларни техники имаат дозволено попрецизна идентификација на HLA-DR и DQ алели што и предиспонираат на МС.
Првите разлики на различни HLA алели беа направени со користење на рестриктивниот ензим Tag1 (Olerup et al., 1989); потоа беа употребени други рестриктивни ензими. Alleles сега се дефинираат со користење на специфични олигонуклеотиди за препознавање на специфичните низови, пропратено со полимеризирачка верижна реакција (ПВР). Со овој метод хаплиотипот што специфично и предиспонира на МС кај Европјаните е опишан како ДРБИ*1501-DQAI*0102-DQBI*0602 (Spurkland et al., 1991; Olerup and Hillert, 1991). Можно е DR7 и DQBI*0303 да даваат извесна заштита на развојот на МС ( Spurkland et al., 1991; Kally et al., 1993). Интересно е што овие HLA alleles се појавуваат да влијаат на текот на МС ( дали хронична и прогресивна или повратна или одложена; Olerup et., 1989; Olerup and Hillert, 1991 ), како и тоа дали пациентот со изолирана повреда ќе продолжи да развива понатамошна евиденција на МС (Kelly et al., 1993 ). Овие ХЛА молекули од класа II се високо полимерни и се блиску инволвирани со презентирање на антиген од Т ќелии и поради тоа до производството на антитела од ќелиите.
Не е изненадувачко тоа што тие се имплицирани во етиологијата на автоимуните болести, како титоидитис, тип I на diabetes mellitus и myastheria gravis. Можно е патогенезата на МС да се инволвира, бидејќи антителата до миелинскиот основен протеин се најдени во CSF на пациентите ( Catz and Warren, 1986) и на неговите 13> ќелии ( Olsson et al., 1990 ). Меѓутоа, антителата на нервното ткиво не се најдени во крвта на пациентите со МС.
5.1 Други предиспонирачки гениИсто така и други гени влијаат на развојот и текот на МС. Ова е сумирано во еден обемен преглед од Oksenberg et al., (1993). Бидејќки имуната регилација повлекува партнерство помеѓу класа II HLA аллели и Т-келиските рецептори, беше сфатено дека полиморфизмот во Т-келиските рецептори гените можат да влијаат на осетливоста на МС, бидејќи беше сознаено дека Th1 поттипот кај глувците што му предиспонира на експерименталниот алергичен енцефаломиелитис има хомологии со Т-келискио поттип најден кај пациентите со МС (Voskuhl et al., 1993 ). Оксенберг ет ал., (1989) и Беалл ет ал., (1989) покажаа дека извесни полиморфизми и од А- и од Б- веригите на Т-келискиот рецептор се значително поопшти кај пациентите со МС отколку кај соодветните контроли. Други студии покажаа конфликтни резултати ( види преглед од Oksenberg et al., 1993). Може да биде една причина за конфликтот поради реакција помеѓу специфичен HLA аллеле и специфичен полиморфизам на Б-верига на Т-келискиот рецептор ( Beall et al., 1993). Студијата изведена од Seboun et al., (1989) го подржува инволвирањето на Б-верижните гени во рзвојот на МС, бидејки ова покажува значително искривена дистрибуција на Б-верижните хаплотипи во парови на заразени родени браќа или сестри. Така, односите на заразените браќа или сестри кои што делат 2, 1, или 0 хаплотипи се 0.38, 0.55, 0.08 соодветно наместо 0.25, 0.50, и 0.25.
Постои исто така индиректна евиденција дека варијацијата во миелинскиот базен протеин генот може да предиспонира на осетливоста на МС, бидејќи соседниот ДНА маркер е поопшт од очекуваното кај МС пациентите од Британска Колумбија и Финска, отколку кај контролите (Boylan et al., 1992).
Постои исто така евиденција за други гени кои што допринесуваат кон развојот на МС. На пример, аллелес кај цомплемент лоци кои лежат во ХЛА комплексот можат да играат некоја улога. Trouillas and Bethel (1977) опишале hypocomplementemia со ниски циркулирачки нивоа на Ц3 и/или пропердин фактор Б кај 75 пациенти со МС. Абнормалностите во овие фамилии беа врзани со HLA-Б18. Спротивно на тоа, пациентите со нормални серумски нивоа на дополнување покажаа значително здружување со HLA-B7. Trtouillas and Bethel (1977) запазија дека МС пропратена со хипокомплементемиа зема упатувачки тек со релативно бенигни резултат и има историја на чести инфекции пред развојот на МС.
Fielder et al., (1981) проучувал 135 студенти од кои 45 имале оптички неуритис без прогресија кон МС. Пациентите кои продолжиле кон МС имаат значително пониска фрекфенција на Fallele на пропердин фактор Б, сугерирајши дека овој allele може да има дејство во заштита против понатамошни епизоди на демиелинација. Иако овој ефект не беше виден во следна студија на истите пациенти 6 години подоцна, кога повеќе развија МС (Francis et al., 1987), една студија од Финска (Ilonen et al., 1983) покажа дека пациентите со МС тежнеат кон недостаток и на HLA-Dwl allele и кон F allele на пропердин фактор Б. Значи, сеуште изгледа веројатно дека комплементарните алели играат извесна улога во етиологијата на МС.
Понатамошна евиденција за ова доаѓа од една студија на 13 фамилии на вишеструк случај, во кој постои врска помеѓу А4Б2 хаплотип на Ц4 и случај на МС (Сцхродер ет ал., 1983).
Генетичките полиморфизми на други хромозоми изгледа се поврзани со МС, како што е претскажано од Ho et al., (1982). Еден од овие е имуноглобулинскиот тежок низ (Gm) алотип. Различни алотипи се соопштени како прекумерно чести кај МС пациентите (Pandey et al., 1981 ; Stewart and Kirk, 1983 ; Blanc et al., 1986 ; Francis et al., 1986).
Слаб ефект на АБО Резус крвните групи можат да бидат ефикасни исто така (McDonald et al., 1976). Пп2 типот на интестинален алкалиин фосфат е помалку вообичаен од очекуваното кај МС пациентите (Papiha and Roberts, 1975), сугерирајќи дека овој алел, како пропердин БФ алел има заштитно дејство против развојот на МС.
Епидемиолошката евиденција од епидемијата на МС и од нејзината преовладливост кај осетливите индивидуи после миграцијата (Kurtzke, 1983 ; Kurtzke and Hyllested, 1986) покажува дека едно инфективно средство е инфицирачки фактор за МС и дека ова веројатно е ендемично кај извесни популации. Студиите на фамилијата ја подржуваат идејата на една инфекција рано во животот поради високиот степен на согласност кај МЗ близнаците и степен на согласност кај ДЗ близнаците кој е повисок од оној кај родените браќа или сестри. Овие студии за близнаците сугерираат дека не е само изложеноста (можеби повеќе од еден пат) на инфективно средство важна, туку исто така тајмингот на вакво изложување е критично. Најверојатно, имунолошкиот статус на детето на изложеност е важен и ова е најверојатно слично кај близнаците кои се изложени на антигени стимуланси на истите возрасти. Студиите на заразени парови го потврдуваат постоењето на општ МС предиспонирачки ген, поважен кај жените отколку кај мажите, во HLA комплексот, но ова не е важно за развојот на МС. Други генетички полиморфизми исто така изгледа се етиолошки важни кај некој пациенти.
Постоењето на разни предиспонирачки гени прави веројатност дека полигенското наследство оперира и дека е потврдено од дистрибуцијата на МС кај фамилиите. Предиспонирачките гени изгледа дека се од различна важност кај различни пациенти и кај различни раси.
ЗЛКЛУЧОК
МС е добар пример на болест со полигена предиспозиција. Алелите кај многу локуси допринесуваат за развојот на болеста, кога еднаш ќе се случи една битна инфекција (или серија на инфекции). МС е исто така пример на болест кај која се објаснети степените на висока согласност кај близнаците, не само со генетички фактори туки и со фактори на околината.
ЛИТЕРЛТУРA
1. Human Genetic Vol.2
Multiple Sclerosis and Other Demyelinating Disorders - Sarah Bundey
2. Klinicka neurologija, B. Radojcic
3. OMIM, on-line Mendelian in Man
Слика 1Co црно - ареи co преваленција од 30 или повеќе случаи на 100 000 жители
Со точки - ареи со преваленција 5 - 29 случаи на 100 000 жители
Со коси црти - ареи со 5 случаи на 100 000 жители
Табела 1: Превенција на MC кај роднини
Табела 2: MC кај близнаци
Табела 3: Преваленција на MC во популацијата и кај близнаците
Besplatni Seminarski Radovi - Бесплатно семинарска работа